Etiquetado: apetito
El apetito mágico
GHRELIN is a hormone made in the stomach that causes hunger. (David Ludwig)
La ghrelina es una hormona producida en el estómago que causa hambre
O quizá no es así.
«Enhanced responsiveness of Ghsr Q343X rats to ghrelin results in enhanced adiposity without increased appetite«
Experimento con ratas que tienen una mutación genética que las hace más sensibles a la ghrelina, la «hormona del hambre». Se supone que esas ratas tienen que tener un gran apetito, se supone que tiene que haber «hiperfagia» (o sea que coman mucho) y se supone que tiene que haber aumento de peso.
GhsrM/M rats displayed enhanced responses to submaximal doses of ghrelin or GHSR agonist.
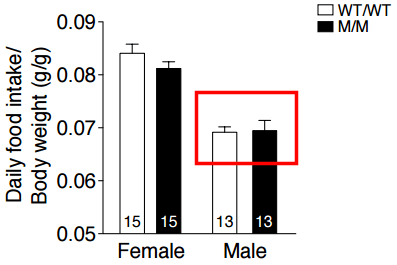
Pero las ratas no comieron más que las ratas sin esa mutación (grupo WT). En la gráfica se muestra la ingesta energética (normalizada con el peso corporal):
Although GhsrM/M rats showed enhanced growth hormone secretion and food intake to submaximal doses of agonist, these animals are neither giants nor hyperphagic.
… ni gigantes ni hiperfágicas.
Pero, ¡oh sorpresa! las ratas sensibles a la ghrelina sí ganaron grasa corporal:
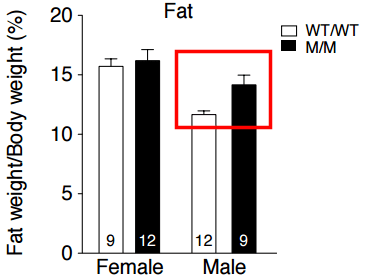
La hormona del apetito engorda sin hacer que comas más…
Quite surprisingly, for a so-called orexigenic hormone, these animals were not eating more proportionally compared to their wild-type counterparts (fuente)
De forma bastante sorprendente para una hormona supuestamente estimuladora del apetito, estos animales no comieron más en comparación con los animales normales
O quizá no hay magia y lo que sucede es que se ha estado confundiendo una asociación con una relación causa-efecto. A lo mejor la ghrelina es uno de los mecanismos fisiológicos por los cuales en una situación de hambre nuestro cuerpo lo que prioriza es acumular grasa corporal. Y un efecto secundario puede ser que al estar engordando, quizá tengas un poco más de apetito. En tal caso, sólo si se administra una dosis extraordinaria de ghrelina habría claros efectos en el apetito, que es justo lo que se observa:
in both control and ghrelin cell-ablated mice, only supraphysiological doses of ghrelin could stimulate food intake. Collectively, these observations support that ghrelin is not a regulator of food intake in rodents in standard housing conditions. In contrast, our results emphasized the role of ghrelin in fat storage, which is in agreement with previous observations supporting that both adipogenic and orexigenic roles of ghrelin are independently regulated
tanto en ratones control y como en ratones cuyas células carecen de ghrelina, sólo las dosis suprafisiológicas de ghrelina fueron capaces de estimular la ingesta de alimentos. En conjunto, estas observaciones apoyan que la ghrelina no es un regulador de la ingesta de alimentos en roedores en condiciones de vivienda estándar. En contraste, nuestros resultados enfatizaron el papel de la ghrelina en el almacenamiento de grasa, que está de acuerdo con observaciones anteriores que apoyan que los papeles adipogénicos y estimuladores del apetito de la ghrelina son regulados de forma independiente
«sólo las dosis suprafisiológicas de ghrelina fueron capaces de estimular la ingesta de alimentos […] estas observaciones apoyan que la ghrelina no es un regulador de la ingesta»
«Nuestros resultados enfatizan el papel de la ghrelina en el almacenamiento de grasa«, es decir, una hormona que produce engorde al margen de las calorías y del balance energético, por pasar hambre.
With this in mind, he suggested that the observed peak in ghrelin prior to meals might not be driving the search for food, but instead “preparing an organism to metabolize and store the [incoming] energy.” (fuente)
Con esto en mente, él [Pantel] sugirió que el observado pico de ghrelina antes de las comidas podría no estar empujando la búsqueda de comida sino, en su lugar, preparando el organismo para metabolizar y almacenar la energía [entrante]
«Butyrylcholinesterase Deficiency Promotes Adipose Tissue Growth and Hepatic Lipid Accumulation in Male Mice on High-Fat Diet«
En este otro estudio se comparan ratones normales (WT, wild type) con ratones a los que se les ha reducido una enzima secretada por el hígado que reduce los niveles de ghrelina (BChE KO). Se ha reducido algo que reduce… un poco liososo, sí. En resumen, en el grupo BChE, el de intervención supuestamente esos ratones tenían que tener más hambre que los WT y por tanto, según la charlatanería del balance energético, engordar más. Pero en los primeros meses los ratones BChE ¡engordaron más sin comer más!

Y los autores así lo constataron: no hubo diferencias en la ingesta energética, pero la ganancia de peso fue diferente.
Initially, we saw no apparent difference in food intake with or without vector treatment, but food powder lost into bedding was not accounted for. More rigorous measures of food intake were then made on a daily basis with 2 cohorts of single-housed mice. One group was young (3 mo old) and had fed only on regular chow. Their average weight at this point was slightly higher than WT but not different by t test. However, a significant weight divergence emerged over the next 2 weeks on high-fat diet, P < .05 by two-way ANOVA (Figure 2A). This divergence grew further during 4 more months of HFD (Figure 2B), and it was sustained or enhanced at 9 months, the study endpoint (Figure 2C). Energy intake in the younger KO mice did not differ measurably from that in same-age wild-type controls (Figure 2D)
«Inicialmente no vimos diferencias en la ingesta de comida […] Sin embargo apareció una diferencia en el peso corporal»
Según la pseudociencia del balance energético, si el peso corporal aumenta la causa es que has comido más de lo que has gastado, así que los autores del experimento también barajaron la posibilidad de que un reducido gasto energético hubiese contribuido al aumento de peso de los ratones KO:
Because increases in body weight imply an excess of energy intake over energy expenditure, we examined the possibility that decreased energy expenditure contributed to excess fat gain in KO mice.
Y, aunque no encontraron diferencias en el gasto energético (una vez normalizado), les importó un pimiento para de ello concluir que un gasto energético reducido era la causa más probable de la acumulación de grasa en los ratones KO:
reduced overall energy expenditure seemed the most likely cause of increased fat accumulation in the KO mice.
Acumular grasa corporal es una cuestión matemática —¡claramente!— porque todos sabemos que los seres vivos funcionamos según una resta de dos valores:
The higher fat burden in BChE KO mice clearly reflects excess of energy intake over outgo.
Por cierto, estas patochadas caloréxicas están publicadas en la revista «Endocrinología»…
«Butyrylcholinesterase gene transfer in obese mice prevents postdieting body weight rebound by suppressing ghrelin signaling«
En este otro artículo, de los mismos autores que el anterior, se observa que suprimir la señalización de la ghrelina reducía la ingesta al tiempo que limitaba la recuperación del peso perdido tras tres semanas de restricción calórica. ¿Qué conclusiones pueden sacar unos «científicos» que confunden una tautología con una relación causa-efecto?
Body weight is controlled by the central nervous system, as peripheral hormonal signals integrate in the hypothalamus to regulate food intake and energy outgo
El peso corporal es controlado por el sistema nervioso central, ya que las señales hormonales periféricas se integran en el hipotálamo para regular la ingesta de alimentos y la salida de energía
Pues eso, para ellos estaba claro que era comer menos lo que había limitado la ganancia de peso. Pero la relación causa-efecto sólo está en la imaginación de los autores del estudio. En el artículo que hemos visto antes «sabían» que lo de la ghrelina no era tan sencillo como que hace comer más o menos (ver):
Animal research confirms that ghrelin is a hunger-stimulating hormone, but ghrelin-induced overeating typically requires nonphysiological doses (35, 36) and neither ghrelin KO nor ghrelin receptor KO cause decreased food intake and body weight on normal diets
«el aumento de la ingesta inducido por ghrelina requiere típicamente de dosis no fisiológicas»
O en otras palabras, la hormona del hambre no parece ser una hormona del hambre.
La intervención no era «comer menos»: era un cambio hormonal en una hormona que tiene efectos engordantes que los autores saben que también existen en ausencia de cambios en la ingesta energética. Y además es un resultado en ratones. Pero ellos lo interpretan para promocionar la fantasía caloréxica de que si los humanos comiéramos «menos» tras haber perdido el peso, podríamos evitar el efecto rebote:
Our study targeted postdieting hyperphagia with an effective approach based on BChE gene transfer to suppress appetite-promoting signals, prevent weight rebound, and promote long-term healthy body weight.
Es tan sencillo como hacer el experimento: sometemos los ratones a restricción calórica y luego les limitamos la cantidad de comida para que no se pasen comiendo. Pero esos experimentos ya existen y el resultado debería servir para olvidar de una vez esa estupidez de intentar perder peso pasando hambre. Aunque sólo fuera por su largo historial de fracasos.
Reflexiones finales
Más relevante que el hecho de que sea correcta o no esta idea sobre la ghrelina me interesa la hipótesis: si se engorda más por la activación de la «hormona del hambre» sin que exista un aumento de la ingesta, podemos interpretar estos resultados como acumular más grasa corporal por el hecho en sí de tener hambre (y al margen de las calorías).

El argumento de que las dietas dejan de funcionar porque el gasto energético se reduce es dar por buena la pseudociencia del balance energético. Como mínimo habría que explicar por qué se asume que ésa es la causalidad según la cual funciona nuestro cuerpo. Y explicar por qué se descartan sin más otras posibles causalidades (ver,ver).
Como nota final, los niveles de ghrelina en sangre aumentan al tratar de adelgazar con una dieta hipocalórica (ver,ver,ver,ver,ver). Interesante, ¿verdad?
Leer más:
