Etiquetado: enfermedad autoinmune
Trigo y sistema inmune (3 de 4)
«Higher constitutive IL15Rα expression and lower IL-15 response threshold in coeliac disease patients«
Los autores nos explican que, en el modelo más aceptado de cómo se inicia la celiaquía, la gliadina desencadena una reacción innata caracterizada por la producción de interleucina 15 (IL-15) por parte de las células epiteliales:
gliadin toxic peptides (i.e. the 19-mer) trigger an innate immune response [10], mainly characterized by the production of IL-15 by epithelial cells
En este estudio encontraron que el sistema inmune de la mitad de las personas no celíacas percibe el gluten como un antígeno y se pone en marcha el sistema inmune innato segregando IL-15. Los autores interpretan textualmente esa observación como «dañino efecto«:
The data obtained in this pilot study support the hypothesis that gluten elicits its harmful effect, throughout an IL15 innate immune response, on all the individuals. This innate response is found in both patients with and without CD, although the triggering of an adaptive response is CD specific. (fuente,fuente)
La hipótesis de los autores es que las personas que sufren celiaquía necesitan niveles más bajos de la IL-15 para desencadenar la respuesta adaptativa, lo que explicaría que ellos sí tengan una respuesta inflamatoria cuando lo cierto es que el gluten no sólo produce la reacción del sistema inmune innato en esas personas:
The results shown here, the increased expression of both IL15Rα and pro-inflammatory mediators, and the higher response to IL-15, support the hypothesis that CD patients have a lower IL-15 threshold response. This hypothesis may explain why the (innate) IL-15-mediated response to gluten is not restricted to CD, though the secondary inflammatory response is only observed in genetically susceptible CD patients.
«Intestinal cell damage and systemic immune activation in individuals reporting sensitivity to wheat in the absence of coeliac disease«
En este estudio encontraron que las personas que sin ser celíacas decían tener sensibilidad al gluten tenían indicadores de translocación microbiana más elevados.
we measured the levels of LBP and sCD14 as indicators of the translocation of microbial products, particularly LPS, across the epithelial barrier. […] We found significantly elevated serum levels of both LBP and sCD14 in individuals with NCWS in comparison with patients with coeliac disease and healthy controls.
Lo que según ellos sugiere que la translocación de productos desde el tracto intestinal contribuye a la activación del sistema inmune innato y adaptativo observada en las personas que tenían sensibilidad al gluten no celíaca:
We found that levels of IgG and IgM antibodies to flagellin were significantly elevated in the NCWS cohort. Considering that no individuals in this study had evidence of infection, these observations are suggestive of a translocation of microbial products from the GI tract that contributes to the observed innate and adaptive immune activation in the NCWS cohort
Y cuando esos sujetos seguían una dieta sin trigo (o cereales relacionados) los marcadores de activación inmune, los marcadores de daño epitelial en el intestino y los síntomas mejoraban:
we examined the above markers in a subset of NCWS subjects before and after a diet that excluded wheat and related cereals. The results indicated a significant decline in the markers of immune activation and gut epithelial cell damage, in conjunction with the improvement of symptoms.
«The Prevalence of Antibodies against Wheat and Milk Proteins in Blood Donors and Their Contribution to Neuroimmune Reactivities«
Los datos de este artículo muestran que un notable porcentaje de personas presenta anticuerpos frente al trigo, es decir, una reacción del sistema inmune adaptativo ante los distintos antígenos del trigo.
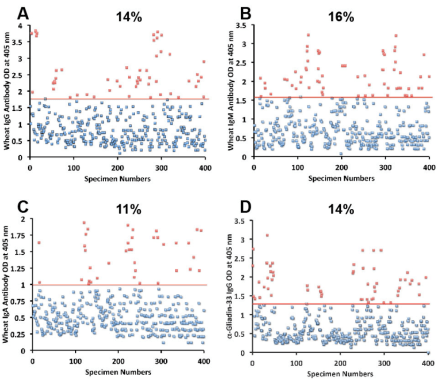
Además en este estudio se encontró una gran coincidencia entre generar anticuerpos contra el gluten o la leche y generar anticuerpos contra proteínas del propio cuerpo:
Statistical analysis showed significant clustering when certain wheat and milk protein antibodies were cross-referenced with neural antibodies. Approximately half of the sera with antibody elevation against gliadin reacted significantly with GAD-65 and cerebellar peptides; about half of the sera with elevated antibodies against α + β-casein and milk butyrophilin also showed antibody elevation against MBP and MOG.
La gráfica muestra una análisis de grupos de dos vías de los coeficientes de correlación de Pearson entre proteínas de la comida y proteínas del cerebro:

¿Un resultado causado por la reactividad cruzada?
This cross-reactivity between α-gliadin and cerebellar peptides, and between milk butyrophilin and MOG peptides, could be responsible for the simultaneous detection of antibodies against these molecules in a small percentage of tested blood samples.
Ante estos resultados los autores plantean la posibilidad de que debido al «mimetismo molecular» entre el gluten y algunas proteínas del cuerpo, especialmente proteínas del sistema nervioso, la respuesta inmune ante el trigo acabe produciendo un problema neuroinmune en un pequeño porcentaje de personas:
With these experiments we demonstrated that cerebellar and MOG peptides, which are known to be important autoantigens in gluten ataxia and MS, can cross-react with wheat and milk proteins. The demonstration of molecular mimicry between α-gliadin, cerebellar peptide, milk butyrophilin, and MOG, and the simultaneous detection of antibodies against these proteins in a small percentage of the general population may have broader implications in the induction of neuroimmune disorders. In these individuals, due to a regulatory defect in mucosal immunity, the consumption of wheat and milk products provides a source of α-gliadin, γ-gliadin, and milk butyrophilin-derived peptides that can cross the gut mucosa to stimulate antigen-specific immune responses both locally in the gut as well as in the periphery. In the majority of the population the cerebellar and MOG normally remains sequestered behind the blood brain barrier (BBB). However, CNS inflammation and BBB breakdown can render the neural tissue antigens accessible to the cross-reactive antibodies and auto-reactive lymphocytes, subsequently resulting in neuroimmune disorder
Según uno de los autores del artículo, las personas con sensibilidad al gluten y los lácteos tienen un riesgo mayor de lo que se creía de desarrollar una enfermedad autoinmune neurológica:
those with a gluten and dairy sensitivity have a much higher risk of developing neurological autoimmunity than previously suspected (fuente)
«Correlation of Tissue Antibodies and Food Immune Reactivity in Randomly Selected Patient Specimens«
En la figura se muestra el mecanismo de reactividad cruzada que puede llevar a autoinmunidad: el cuerpo genera anticuerpos contra el gluten (gliadina) pero parte de esos anticuerpos confunden tejido del cerebelo con el gluten y se produce la neuroautoinmunidad.

Según los autores del artículo, el mecanismo de reactividad cruzada que acabamos de ver deja claro cómo de potencialmente dañina para el cuerpo humano es la gliadina, es decir, el gluten:
With this information, it is clear how potentially damaging gliadin can be to the human body.
En la siguiente gráfica se aprecia cómo el porcentaje de personas con anticuerpos IgG frente al gluten (gluten positive) que también tienen anticuerpos contra las propias proteínas del cuerpo es mucho mayor que en la población que no desarrolla anticuerpos contra el gluten (gluten negative).
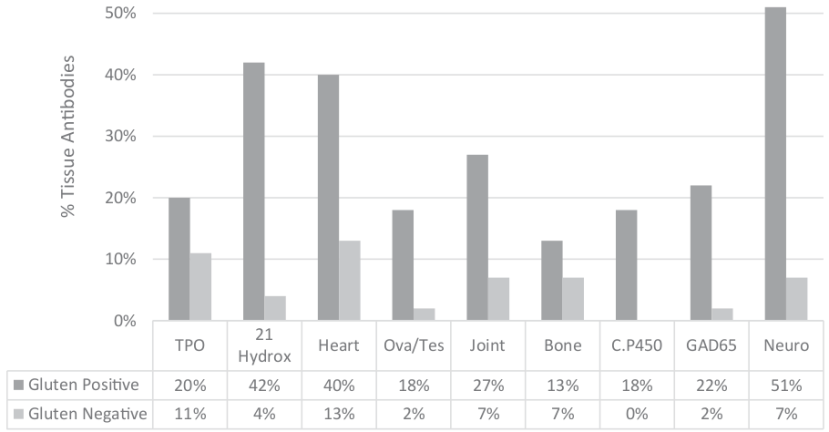
Los autores del artículo resaltan que los médicos no han entendido todavía que no son los celíacos los únicos que deben ser estrictos con una dieta sin gluten, pues el daño en las personas que tienen sensibilidad al gluten no celíaca puede ser tan grave como el que sufre un celíaco:
Interestingly, the gluten-free diet (GFD) is generally recommended for specific autoimmune disorders, as the GFD may reduce systemic inflammation, cut down on the frequency of flares, or arrest the autoantibody production against targeted tissues [49-52]. Unfortunately, much of the clinical world has not yet grasped the idea that gluten can trigger autoimmune disorders other than CD, which leads to misleading notions that only CD patients have to be strict with the gluten-free diet (GFD), while NCGS patients can “cheat” once-in-a-while. Statements such as, patients with “NCGS can be more liberal and titrate their exposure to gluten as needed to avoid symptoms,” [53] can be harmful to the patient. CD is a gastrointestinal disorder in which patients make elevated IgA to gliadin and tissue transglutaminse-2. What if the NCGS patient makes significant levels of IgG against gliadin and cerebellar protein? Is protecting the brain really less important than protecting the gut?
Los autores del artículo resaltan que la prevención de la autoinmunidad de causa dietaria es posible: basta con retirar de la dieta la sustancia que detona el proceso autoinmune:
There are three main ingredients for environmentally-induced autoimmunity, genetic susceptibility, dysfunctional body barrier and environmental trigger [75-78]. If the environmental trigger is removed, even with a broken body barrier and a genetic susceptibility, autoimmunity can be evaded. Alternatively, if the environmental trigger, in our case, food protein is still present, once the intestinal barrier has been breached, the offending food protein ignites the immune system and pathogenesis begins its slow progression toward tissue damage. Autoantibody biomarkers can be detected at this point. A patient is at greater risk for developing a disease, if certain markers are present and the more detectable markers, the higher the positive predictive value for disease [79,80]. Prevention of environmentally-induced autoimmunity is possible.