La fisiología de engordar (5 de 9)
El propósito de esta quinta parte del artículo es detallar la secuencia temporal de acontecimientos que hace que entre/salga grasa en los adipocitos.
Aquí y ahora, al son que marca la insulina
En la imagen se muestra, tras una comida, la evolución de concentraciones plasmáticas de triglicéridos y glucosa (ambos en parte superior) y de insulina y ácidos grasos libres (ambos en parte inferior). Describo la secuencia de acontecimientos tras la figura.
En paralelo, lo primero que sucede es que:
- por un lado llegan a sangre las lipoproteínas, procedentes de la comida y del hígado (quilomicrones y VLDL, respectivamente), y
- la comida produce una elevación de la glucemia y con ella de la insulinemia.
La LPL (liproteína lipasa) se activa en respuesta a la subida de la insulina y hace que las lipoproteínas se anclen al endotelio (proceso que en inglés se llama margination, que podríamos traducir como «apartamiento», ver,ver) para vaciar su contenido. Por un lado los triglicéridos en sangre aumentan por la incorporación al torrente sanguíneo de nuevas lipoproteínas, y, por otro lado, se reducen porque la LPL los vacía y se generan ácidos grasos libres en plasma. Gran parte de esos ácidos grasos liberados son captados por el tejido adiposo, lo que explica el descenso en la concentración de ácidos grasos en sangre (gráfica abajo a la derecha). No obstante, parte (25-75%, ver,ver,ver) de los ácidos grasos libres procedentes de las lipoproteínas no entran en el tejido adiposo y quedan en el plasma, lo que en parte explica el aumento de la concentración plasmática de NEFA a partir de los 90 min. Quizá una explicación de por qué se produce ese derrame o spillover es que a partir de cierto momento los niveles de insulina ya han decrecido considerablemente y los adipocitos ya no van a esterificar los ácidos grasos que ya se hayan sacado o que se saquen a partir de ese momento de las lipoproteínas (ver,ver). Siguiendo con la subida de la concentración de NEFA, a ella contribuye de otra forma la reducción en la insulinemia, pues produce liberación de ácidos grasos por parte de los adipocitos (ver). En la gráfica de los NEFA (gráfica anterior, abajo a la derecha), 4h tras la comida la concentración de ácidos grasos en sangre (ligados a albúmina) ya se ha recuperado el nivel previo a la ingesta.
La entrada directa de grasa dietaria en el tejido adiposo guarda relación con la elevación postprandial de la insulina (ver):
 |
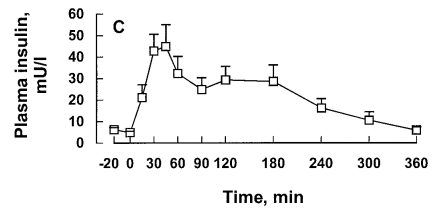 |
La siguiente gráfica es muy ilustrativa sobre cómo la elevación de la insulina (puntos blancos) reduce la concentración de ácidos grasos libres en sangre (puntos negros), que son capturados de forma neta por el tejido adiposo (absorbe más y suelta menos):
Plasma NEFA concentrations therefore fall after any meal that contains carbohydrates, which stimulate insulin release (fuente)
Las concentraciones de NEFA [ácidos grasos no esterificados] se reducen tras cada comida que contiene carbohidratos, los cuales estimulan la liberación de insulina
Durante las 5 horas siguientes a una comida (i.e. mientras la insulina permanece elevada) hay entrada neta de ácidos grasos en el tejido adiposo (es la interpretación de que los puntos negros estén por encima del nivel 0 en la siguiente gráfica). Si hacemos tres comidas fuertes al día nos podemos pasar todo el tiempo que estamos despiertos en estado postprandial y almacenando grasa de forma neta (ver).
Me parece muy relevante cuándo suceden las cosas y por qué. El tejido adiposo no espera a ser informado del «balance energético» total del cuerpo al final de ese día para saber cuánta grasa corporal tiene que almacenar. De hecho, el tejido adiposo nunca recibe información sobre el «balance energético»: almacena grasa de forma neta en el periodo postprandial según le marcan las hormonas, fundamentalmente la insulina (ver) y la presencia de sustratos. Pero lo que quiero resaltar es el cuándo: ante una comida, el tejido adiposo actúa en primer lugar, que es justo después de comer, cuando se eleva la insulina en el período postprandial, mientras que el resto de órganos/tejidos procederán a partir de ese momento a gestionar lo que no ha entrado en el tejido adiposo. Tampoco esos otros órganos/tejidos esperarán a conocer el «balance energético» total del día para actuar: eliminarán los ácidos grasos sobrantes en cuanto estos entren en las fibras musculares por mecanismos activos o pasivos y empiece a haber demasiados ácidos grasos para las necesidades de ATP de las células musculares. O puede que no sea realmente así, pero es lo que yo veo que sucede.
This process of spillover describes FA released by intravascular lipase activities (lipoprotein lipase and/or hepatic lipase) that were not channeled efficiently to direct uptake at the site of lipolysis and are thus released into venous circulation (53). In the process of spillover, FFA become systemically available and can ultimately be used by tissues after recirculation through the arterial vasculature (fuente)
En el proceso de spillover, los ácidos grasos pasan a estar disponibles para todo el sistema y pueden en cualquier momento ser usados por los tejidos una vez son recirculados por la vasculatura arterial.
Otro dato relevante en la gráfica anterior es que en personas con obesidad (círculos blancos) apenas entra grasa en los adipocitos durante el día (o más bien en los periodos postprandiales) y apenas sale grasa por la noche (o más bien cuando pasan unas horas tras la última comida). El dato es por unidad de masa grasa, pero al tener más masa grasa el comportamiento global del cuerpo no es muy diferente del de una persona delgada.
Lo que ha sobrado puede ser eliminado
Nótese que los ácidos grasos se están elevando en las dos últimas horas de las gráficas anteriores. ¿Cuáles son los mecanismos que regulan que esos niveles no se disparen, por ejemplo por sucesivas comidas altas en grasa o por una lipólisis aumentada en el tejido adiposo?

Parece lógico pensar que como parte de la regulación de la concentración de ácidos grasos libres en sangre (NEFA o FFA), existe un mecanismo fisiológico que si detecta excesivos ácidos grasos en plasma se encarga de eliminarlos y su energía es disipada en forma de calor. En tal caso, parte de lo que no sea almacenado en el tejido adiposo inmediatamente tras la comida va a incrementar esos niveles de NEFA plasmáticos y, por tanto, influirá en cuántos ácidos grasos acaban siendo disipados en forma de calor.
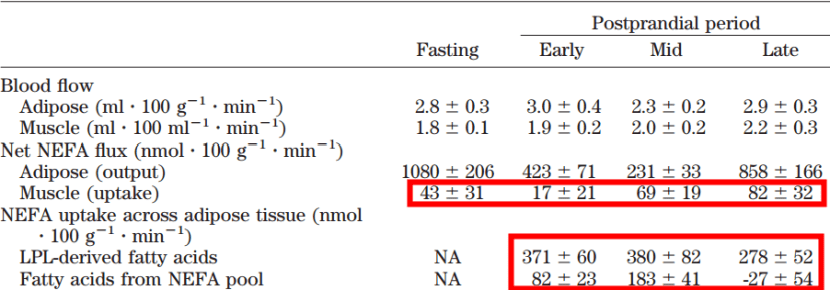
Por ejemplo, fijémonos en los datos de este estudio:
Como vemos, el tejido muscular incrementa su absorción de ácidos grasos en el periodo postprandial, en parte para eliminarlos como calor y coincide que esa activación se produce cuando los niveles suben y no sucede cuando están bajando. Y el otro dato relevante es que lo que entra en el tejido adiposo en el periodo postprandial viene principalmente de las lipoproteínas, pero también algo de los ácidos grasos que hay en plasma. Si se acumulan en plasma y ningún órgano (e.g. el tejido muscular) los retira de ahí es lógico pensar que el tejido adiposo acabe acumulando más grasa y ayude así a mantener los NEFA en concentraciones normales. Es una posibilidad.
Una vez baja la insulina, la musculatura esquelética aumenta la obtención de ácidos grasos a partir de las lipoproteínas en plasma:
The LPL response to feeding and fasting is also tissue specific. In rodents and humans, this regulation in white adipose tissue and muscle exists mostly at the posttranslational level. Adipose tissue LPL activity is high after feeding and low during fasting, whereas in most studies, the opposite is true in the heart and skeletal muscle […] Insulin is a major regulator of LPL activity in adipose tissue.
La respuesta de LPL a la alimentación y al ayuno es también específica del tejido. En roedores y seres humanos, esta regulación en tejido adiposo blanco y músculo existe sobre todo en el nivel posttraduccional. La actividad de la LPL del tejido adiposo es alta después de alimentarse y baja durante el ayuno, mientras que en la mayoría de los estudios, lo contrario es verdad en el corazón y el músculo esquelético […] La insulina es un regulador importante de la actividad de LPL en tejido adiposo.
Ideas
- El tejido adiposo actúa en primer lugar, captando tantos ácidos grasos como las hormonas y la presencia de sustratos le marcan
- Lo que no entra en el tejido adiposo puede ser eliminado en forma de calor como parte de la regulación de los niveles de ácidos grasos libres en sangre
- No nos engordaría lo que el resto del cuerpo no gasta de lo que hemos comido, sino que el cuerpo gastaría lo que no nos ha engordado
- El gasto energético de los distintos órganos/tejidos no es constante y no se puede entender si se ignora la actividad del tejido adiposo
Nótese que los procesos de los que estoy hablando (fuga de protones gracias a las proteínas desacopladoras) no son procesos anecdóticos en el ser humano, sino que participan en una parte muy importante de nuestro gasto energético, especialmente los presentes en el tejido muscular:
Uncoupling (proton leak) of the MRC constitutes a considerable part of the RMR (7). Approximately 20%-50% of total energy expenditure is due to proton leaks, with the skeletal muscle as the main contributor (fuente)
El desacoplamiento (fuga de protones) de la cadena respiratoria mitocondrial es una parte importante de la tasa metabólica en reposo. Aproximadamente entre un 20 y 50% del gasto energético total es atribuible a las fugas de protones, siendo el tejido muscular el principal contribuidor
Increased FFA availability plays a role in ectopic fat accumulation (45), insulin resistance (2), hypertension (4), and dyslipidemia (3). It may also exert effects on energy expenditure via sympathetic nervous system (5,46,47), uncoupling protein-3 (48), or peroxisome proliferator–activated receptor-δ (49) activation (fuente)
Una aumentada disponibilidad de ácidos grasos libres (FFA) juega un papel en la acumulación de grasa ectópica, en la resistencia a la insulina, hipertensión y dislipidemia. También podría ejercer efectos en el gasto energético a través de la activación del sistema nervioso simpático, de la proteína desacopladora UCP3 o de la PPAR-δ
Y vamos a ver más resultados experimentales que son muy interesantes.
La fisiología de engordar (9 de 9)
La fisiología de engordar (8 de 9)
La fisiología de engordar (7 de 9)
La fisiología de engordar (6 de 9)
La fisiología de engordar (5 de 9)
La fisiología de engordar (4 de 9)
La fisiología de engordar (3 de 9)
La fisiología de engordar (2 de 9)
La fisiología de engordar (1 de 9)
Leer más:



Efecto de la insulina en la lipogénesis en adipocitos humanos (in vitro);
Estas observaciones plantean la intrigante posibilidad de la regulación nutricional diferencial de la lipogénesis. En el estado de ayuno, los niveles bajos de insulina y los altos niveles de GC endógenos estimularán la lipólisis y al mismo tiempo desactivarán la lipogénesis a través de la fosforilación serina de ACC1, disminuyendo el almacenamiento de combustible y aumentando la disponibilidad de FFA para otros tejidos más activos metabólicamente. A la inversa, en el estado alimentado, los niveles de insulina son altos, y aquí la insulina y la GC pueden actuar juntas para promover el almacenamiento de lípidos
https://www.ncbi.nlm.nih.gov/pubmed/17192479