La fisiología de engordar (4 de 9)
¿Cómo procesa nuestro cuerpo la grasa dietaria?
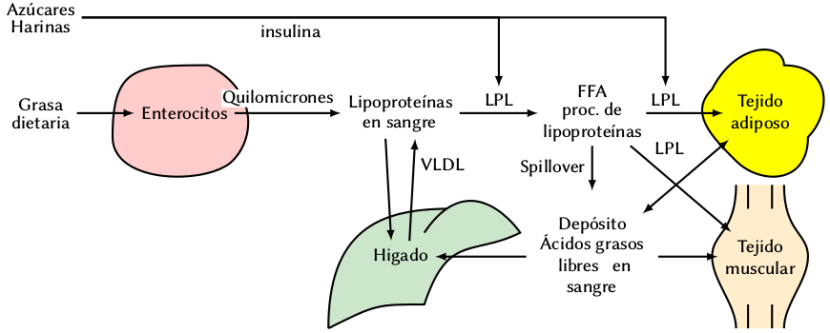
La grasa dietaria es absorbida en el intestino por los enterocitos. Los enterocitos embarcan la grasa en quilomicrones, unas lipoproteínas de gran tamaño (ver), pero no lo hacen en cuanto la absorben sino que guardan en su interior parte de la grasa (quizá la recién ingerida, al tiempo que embarcan en quilomicrones la que ya tienen almacenada, más antigua). No se sabe cuáles son los mecanismos que regulan la generación de los quilomicrones, pero parece ser que están relacionados con la ingesta: la grasa dietaria de una determinada comida es embarcada en quilomicrones también en las siguientes comidas, como parte de una primera fase rápida de aumento en la concentración de los quilomicrones.
Ingestion of a second meal 5 h after the first was shown to produce a very rapid and substantial influx of chylomicron-TAG into the circulation. These chylomicrons contained fat from the first meal (fuente)
La grasa dietaria acaba llegando en quilomicrones a sangre, donde también encontramos grasa embarcada en VLDL (liproteínas procedentes del hígado) y ácidos grasos libres ligados a albúmina, procedentes del tejido adiposo blanco (lipólisis intracelular) o procedentes de las lipoproteínas, en lo que se denomina spillover: son ácidos grasos procedentes de la grasa dietaria que son sacados de las lipoproteínas por la acción de la LPL pero que no acaban entrando en los tejidos sino que se quedan en plasma). Una gran parte de la carga de los quilomicrones, alrededor de la mitad, acaba en el plasma sanguíneo.

This process of spillover describes FA released by intravascular lipase activities (lipoprotein lipase and/or hepatic lipase) that were not channeled efficiently to direct uptake at the site of lipolysis and are thus released into venous circulation (fuente)
En qué proporción los ácidos grasos acaban en el tejido adiposo en el plasma sanguíneo es función del medio hormonal, siendo mayor la fracción de ácidos grasos que van a parar al tejido adiposo cuanto mayores son los niveles de insulina:
There is always an ‘overspill’ of fatty acids into the plasma. Insulin increases the proportion of LPL-derived fatty acids taken up by the tissue but even in the postprandial state typically approx. 50% may be released as NEFA (fuente)
Siempre hay derrame de ácidos grasos a plasma. La insulina aumenta la proporción en que los ácidos grasos sacados por la LPL son captados por el tejido pero incluso en el periodo postprandial típicamente el 50% acaba en plasma como ácidos grasos no esterificados.
El tejido adiposo marrón y el tejido muscular captan grasa de la sangre para convertirla en movimiento o calor, mientras que el hígado recicla ácidos grasos libres y lipoproteínas y las embarca en nuevas remesas de VLDL.
Hechos relevantes:
- La entrada y salida de grasa en el tejido adiposo está regulada fisiológicamente (e.g. insulina). No entra en proporción a las calorías consumidas, sino que la regulación es hormonal y también influirá la mayor o menor presencia de sustratos
- Los niveles de ácidos grasos libres (FFA) en sangre parecen estar regulados. Por ejemplo, aunque están más elevados en los obesos, los niveles tienen el mismo orden de magnitud, a pesar de tener composición corporal y metabolismos muy diferentes. Los puntos negros son de personas delgadas, los blancos de personas con obesidad abdominal (fuente):
- El músculo y el tejido adiposo marrón tienen mecanismos fisiológicos (e.g. proteínas desacopladoras) que pueden eliminar ácidos grasos plasmáticos cuando son excesivos, por ejemplo cuando se detecta que están entrando demasiados por difusión en el músculo. Se libera calor a partir de los ácidos grasos sin obtener ATP. Que exista ese mecanismo fisiológico no implica que se use ni que su acción sea relevante, pero en este artículo del blog presento datos que sugieren que sí es un mecanismo relevante.
Es decir, que la realidad pudiera ser perfectamente que el tejido adiposo almacene la cantidad de grasa dietaria que decida oportuno, en función de los cambios hormonales provocados por la comida y de la presencia de sustratos, y que lo que no se almacene en ese tejido sea gestionado por otros tejidos capacitados para ello. Es decir, que a priori la secuencia de acontecimientos no tiene por qué ser la que establece la teoría del balance energético (ver), sino que puede ser, por ejemplo, la que estoy comentando: el tejido adiposo almacena lo que tiene que almacenar y el resto de órganos se encargan de gestionar lo que ha sobrado.
often plasma NEFA concentrations remain relatively stable as removal by muscle increases to match adipose tissue lipolysis (fuente)
a menudo las concentraciones de NEFA permanecen relativamente estables puesto que el músculo incrementa su retirada de ácidos grasos para equilibrar la tasa de lipólisis del tejido adiposo
These pathways are regulated, most clearly in the case of adipose tissue. Adipose tissue fat storage is stimulated, and fat mobilization suppressed, by insulin, leading to a drive to store energy in the fed state […] Both the liver and skeletal muscle take up fatty acids largely according to their availability. The rate of removal of plasma NEFA is, under most conditions, fairly closely proportional to their plasma concentration (fuente)
Estas vías están reguladas, más claramente en el caso del tejido adiposo. El almacenamiento de grasa en el tejido adiposo se estimula, y la movilización de grasa es suprimida, por la insulina, conduciendo a una propensión para almacenar energía en el periodo postprandial […] El hígado y el músculo esquelético toman los ácidos grasos en gran parte según su disponibilidad. La tasa de retirada de los ácidos grasos plasmáticos está, en la mayoría de las condiciones, bastante de cerca de ser proporcional a su concentración en plasma
Tasa de retirada proporcional a la concentración… interesantísimo (ver).
El spillover y la obesidad
«Spillover of Fatty Acids During Dietary Fat Storage in Type 2 Diabetes«
En este estudio se encontró menos grasa corporal en piernas y tren superior en las personas que tenían mayor spillover.
At baseline, there was a strong negative correlation between spillover and leg fat
High rates of spillover, such as appear to prevail in visceral fat, could represent a mechanism for limiting gain of body fat

Como vemos en el texto citado, los autores del artículo sugieren una relación causa-efecto por la cual que no entre demasiada grasa dietaria directamente en el tejido adiposo en el periodo postprandial puede no ser demasiado engordante. A mí me resulta verosímil que esa grasa «derramada» sea menos engordante y no necesariamente acabe en el tejido adiposo, pues desde el momento en que está en sangre otros órganos/tejidos la pueden disipar como calor.
«Postprandial spillover of dietary lipid into plasma is increased with moderate amounts of ingested fat and is inversely related to adiposity in healthy older men«
En personas mayores y sanas, aumentar la cantidad de grasa en la dieta por un factor 1.74 produjo un mayor spillover (2.3 veces mayor). Además en los participantes se encontró que cuanto mayor era el spillover de la persona, menor era la cantidad de grasa corporal.
Healthy, older participants (63–71 y old) were studied in a randomized, crossover design following ingestions of low (LF) and moderate (MF) amounts of [1,1,1-13C]-triolein-labeled fat, corresponding to 0.4 and 0.7 g of fat/kg body weight, respectively. Spillover of dietary fatty acids into plasma during the 8-h postprandial period (AUC; mmol [middot] L−1 [middot] h) after MF ingestion was 1.2 times greater than that after LF ingestion (2.8 ± 0.4 vs. 1.2 ± 0.1; P < 0.05). The spillover of dietary fatty acids following the MF, but not the LF, ingestion was correlated with the percent body fat (rs = −0.89) and percent body fat-free mass (rs = 0.94) of the men (P < 0.05). After adjusting to the amount of ingested fat, the spillover of dietary fatty acids in the MF trial was disproportionally higher than that in the LF trial

O en otras palabras, las personas a las que «de primeras» el tejido adiposo les captura mayor porcentaje de la grasa dietaria están más gordas. No perdamos de vista que en los tres estudios que presento el resultado es observacional: quizá la causalidad es la contraria y estar más gordo te hace tener menos fracción de spillover. Puede ser.
«Downregulation of Adipose Tissue Fatty Acid Trafficking in Obesity«
Mismo resultado: menor proporción en los NEFA de ácidos grasos procedentes de spillover en hombres con obesidad abdominal que en hombres delgados.
Abdominally-obese men had significantly lower proportion of spillover fatty acids in the NEFA fraction than lean men
Proteínas desacopladoras en el músculo
Las proteínas desacopladoras lo que hacen es convertir los sustratos (e.g. en este caso los ácidos grasos) en calor, sin aprovecharlos para generar «cápsulas» energéticas (ATP). Si las proteínas desacopladoras se activan en la musculatura el músculo se vuelve ineficiente, pues sólo parte de la energía se usa para generar movimiento. Si las proteínas desacopladoras están inactivas, el músculo tiene máxima eficiencia. Que no nos confundan las palabras: cuando de deshacerse de lo que no se necesita se trata, «ineficiente» es bueno. Si fuera cierto que un mayor spillover limitara la ganancia de grasa corporal, la grasa que no entra en el tejido adiposo en el periodo postprandial tendría que ser eliminada de sangre de alguna manera (pues se sabe que los niveles plasmáticos de NEFA no suelen superar ciertos límites). ¿Hay alguna proteína desacopladora en el tejido muscular que aumente tu actividad en presencia de un exceso de ácidos grasos en plasma? Sí, la UCP3:
High fat feeding up-regulates UCP3 in skeletal muscle but not in BAT [96] (Table 3). (fuente)
Pero no me entretengo ahora con la UCP3 y su relación con los ácidos grasos libres. Hablaremos de eso en la sexta entrega del artículo.
Modelos matemáticos de la obesidad basados en la pseudociencia del balance energético
Puesto que una de las patas en las que se sostiene la teoría del balance energético son modelos matemáticos (ver,ver), hago un inciso en esta parte del artículo para contraponer esos modelos con los mecanismos fisiológicos de los que estamos hablando.
El tejido adiposo blanco interactúa activamente con el medio que le rodea, el plasma sanguíneo, captando o liberando más o menos ácidos grasos en función de los niveles hormonales detectados (efectos de LPL/insulina), pero además las concentraciones de ácidos grasos en plasma varían debido a la acción del tejido adiposo y esos niveles afectan a otros órganos, como el músculo y el tejido adiposo marrón, que pueden reaccionar ante un exceso de ácidos grasos eliminándolos y disipando más calor.
Los modelos matemáticos basados en la teoría del balance energético lo que hacen es eliminar el tejido adiposo blanco del sistema modelado, modelando o estimando únicamente el comportamiento energético (que no fisiológico) del resto de órganos. Eso equivale a introducir una premisa en el modelo que va a condicionar los resultados: suponer un comportamiento pasivo, no regulado fisiológicamente, del tejido adiposo, que según esa premisa ni influye ni se deja influir por el medio en el que se encuentra. Esos modelos suponen que la energía que sobra, la diferencia entre lo que ingerimos y lo que los otros órganos/tejidos han gastado, tiene que haber ido a parar al tejido adiposo, que es convertido en un simple receptor «energético» de las sobras del resto del cuerpo.
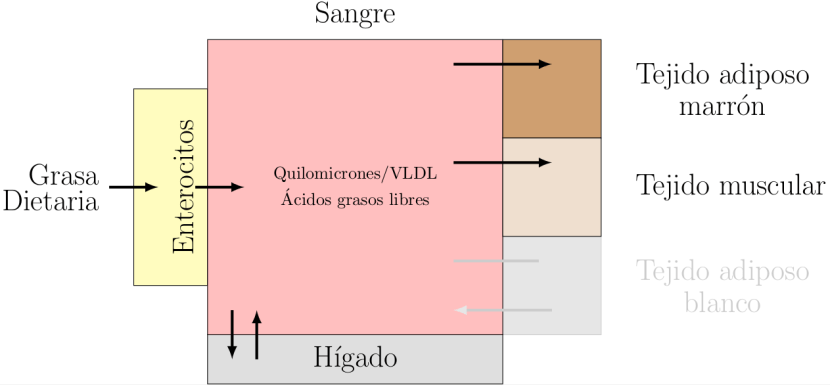
Pero esto es inventarse un comportamiento del cuerpo partiendo de una ley de la física que nada tiene que ver con nuestra fisiología y que consiste en una resta de valores (¿cabe mayor salvajada?). Es posible que el comportamiento de nuestro cuerpo no guarde ninguna relación con lo que supone esa teoría. Por lo pronto, es posible plantear otros comportamientos de nuestra fisiología que también son compatibles con las leyes generales de la física (ver). Un ejemplo de comportamiento sería que gran parte de una comida engordante entra directamente en los adipocitos y el resto (spillover o quilomicrones remanentes) puede ser disipado como calor por otros órganos que cuidan de que las concentraciones de ácidos grasos en sangre no se eleven demasiado (niveles elevados de FFA son tóxicos, ver). Es posible, por ejemplo, que con las mismas calorías una dieta basada en comida real sea menos engordante que otra que quizá sea más baja en grasa y calorías porque entraría grasa en menor medida en un primer momento en los adipocitos y quedarían más ácidos grasos libres en plasma, lo que produciría un marcado aumento de la actividad del resto de órganos (e.g. mediante las proteínas desacopladoras) para regular los niveles plasmáticos de ácidos grasos.
Según la teoría del balance energético, en esta última situación no estaríamos engordando porque no habríamos «comido por encima de nuestro gasto energético«, cuando la realidad habría sido que no se engordaría porque la comida no era engordante y el gasto energético se habría comportado de forma adaptativa, eliminando el exceso de comida. Si el gasto energético de los órganos es adaptativo —¡y lo es!— no se puede despreciar el papel jugado por el tejido adiposo en nuestro cuerpo.
En una persona cuyos tejidos, por genética, tuvieran poca facilidad para activar sus proteínas desacopladoras, los ácidos grasos procedentes del spillover podrían permanecer en sangre más tiempo que en personas genéticamente más afortunadas y esa grasa sería susceptible de ser almacenada en las siguientes comidas del día, cuando subiera de nuevo la insulina.
En definitiva, una teoría o un modelo matemático de la obesidad basados en despreciar la actividad del tejido adiposo no van a poder reproducir la reacción de otros órganos ante los cambios en las concentraciones plasmáticas de hormonas y sustratos que vengan marcados por la actividad del tejido adiposo. Un modelo matemático de la obesidad que no considera el comportamiento fisiológico del tejido adiposo blanco no va a poder reproducir los cambios en la eficiencia muscular causados por la actividad de los adipocitos, del mismo modo que no va a poder reproducir la respuesta del tejido adiposo a los cambios en el medio hormonal. Un modelo matemático de la obesidad en el que no se modeliza el comportamiento fisiológico ¡¡¡¡¡del principal tejido implicado!!!!!, el tejido adiposo, porque se interpreta que así lo permiten hacer las leyes de la física, no es más que charlatanería. Y, en mi opinión, charlatanería con millones de víctimas.
Since the increases and decreases in skeletal muscle UCP2 and UCP3 gene expressions during starvation and refeeding respectively, occur in parallel to the changes in the release of FFA from the adipose tissue into the circulation, the hypothesis was also tested that these changes in circulating FFA, in addition to providing fuel substrate, may also have a role as an inter-organ signal linking the dynamic changes in adipose tissue fat stores to skeletal muscle UCP2 and UCP3 gene regulation. (fuente)
esos cambios en los niveles de ácidos grasos circulantes, además de proporcionar combustible, pueden jugar un papel como señalización entre órganos conectando los cambios dinámicos en los almacenes de grasa corporal con la regulación genética de la UCP2 y UCP3
En la quinta parte de la entrada centraré la atención en cuándo suceden las acciones de nuestros órganos/tejidos relacionadas con acumular grasa corporal. Ser conscientes de cuándo suceden las acciones es relevante para saber por qué actúan los diferentes órganos/tejidos.
La fisiología de engordar (9 de 9)
La fisiología de engordar (8 de 9)
La fisiología de engordar (7 de 9)
La fisiología de engordar (6 de 9)
La fisiología de engordar (5 de 9)
La fisiología de engordar (4 de 9)
La fisiología de engordar (3 de 9)
La fisiología de engordar (2 de 9)
La fisiología de engordar (1 de 9)


En base a lo que se conoce de cómo funciona nuestra fisiología puede ser conveniente no dar bandazos en la composición de nuestras comidas: procesamos mejor una comida cuando su composición es parecida a la anterior. Una posible explicación de ese efecto sería el comportamiento regulador de los enterocitos, que no sueltan de golpe la grasa dietaria consumida en una comida, sino que la racionan entre ésa y las siguientes comidas.
De uno de los artículos que he citado:
Interesantísimo por razones que se entenderán en la séptima entrega del artículo.
No comento nunca pero que sepas que no puedo parar de leer tus Post una y otra vez. Muchísimas gracias por el trabajo que estás haciendo.
Tu blog debería ser de obligada lectura en la carrera de nutrición.
Felicitaciones.
En absoluto: soy yo el que está muy agradecido a todos los que leéis lo que escribo.
He añadido al librito un pequeño resumen de «La fisiología de engordar». Es el Capítulo 3.
https://novuelvoaengordar.com/libro/
Changes in FAT/CD36, UCP2, UCP3 and GLUT4 gene expression during lipid infusion in rat skeletal and heart muscle
Preciosa imagen de gotita de grasa en el interior de un enterocito: